Основные формулы термодинамики и молекулярной физики, которые вам пригодятся. Внутренняя энергия. Работа в термодинамике. Первый закон термодинамики
Энергия любой системы, вообще говоря, зависит не только от свойств самой системы, но также и от внешних условий. Внешние условия, в которых находится система, можно характеризовать заданием некоторых величин, называемых внешними параметрами. Одним из таких параметров, как уже отмечалось, является объем системы, Взаимодействие тел, при котором происходит изменение их внешних параметров, называется механическим взаимодействием, а процесс передачи энергии от одного тела к другому при таком взаимодействии – работой. Термин «работа» используется и для обозначения физической величины, равной энергии, переданной (или полученной) телом при совершении работы.
В механике работа определяется как произведение проекции силы на направление перемещения на величину перемещения. Работа совершается при действии на движущееся тело силы и равна изменению его кинетической энергии. В термодинамике движение тела как целого не рассматривается. Здесь работа, производимая системой (или над системой), связана со смещением ее границ, т.е. с изменением ее объема. Это имеет место, например, при расширении (или сжатии) газа, находящегося в цилиндре под поршнем. При равновесных процессах элементарная работа , совершаемая газом (или над газом) при бесконечно малом изменении объема на определится как
где dh
– бесконечно малое смещение поршня (границы системы), p
– давление газа. Видим, что при расширении газа ( ) совершаемая им работа положительна (
) совершаемая им работа положительна ( ), а при сжатии
), а при сжатии  ) – отрицательна (
) – отрицательна ( ).
).
Таким же выражением определяется работа, совершаемая любой термодинамической системой (или над системой) при бесконечно малом изменении объема. Из формулы (5.4) следует, что если сама система совершает работу (что имеет место при расширении), то работа положительна, если же работа совершается над системой (при сжатии), то совершаемая ею работа отрицательна. Как видим, в термодинамике знаки работы противоположны знакам работы в механике.
При конечном изменении объема от V 1 до V 2 работу можно определить, проинтегрировав элементарную работу в пределах от V 1 до V 2:
 (5.5)
(5.5)
Численное значение работы равно площади криволинейной трапеции, ограниченной кривой  и прямыми
и прямыми  и
и  (рис. 5.1). Поскольку площадь, ограниченная осью V
и кривой p
(V
), различна, то будет различна и термодинамическая работа. Отсюда следует, что термодинамическая работа зависит от пути перехода системы из состояния 1 в состояние 2 и при замкнутом процессе (цикле) она не равна нулю. На этом основана работа всех тепловых двигателей (подробно об этом будет сказано в п. 5.7).
(рис. 5.1). Поскольку площадь, ограниченная осью V
и кривой p
(V
), различна, то будет различна и термодинамическая работа. Отсюда следует, что термодинамическая работа зависит от пути перехода системы из состояния 1 в состояние 2 и при замкнутом процессе (цикле) она не равна нулю. На этом основана работа всех тепловых двигателей (подробно об этом будет сказано в п. 5.7).
Используем эту формулу для получения работы газа при различных изопроцессах. При изохорном процессе V = const, и поэ-
 Рис. 5.1 Рис. 5.1
|
тому работа A
= 0. При изобарном процессе p
= const работа  . При изотермическом процессе чтобы произвести интегрирование по формуле (5.5), следует в ее подынтегральной функции выразить p
через V
по формуле закона Клапейрона – Менделеева:
. При изотермическом процессе чтобы произвести интегрирование по формуле (5.5), следует в ее подынтегральной функции выразить p
через V
по формуле закона Клапейрона – Менделеева:

где  – число молей газа. С учетом этого получим
– число молей газа. С учетом этого получим
 (5.6)
(5.6)
Внутренняя энергия, согласно формуле (5.1), может изменяться как за счет изменения (повышения или понижения) уровней энергии системы, так и за счет перераспределения вероятностей ее различных состояний, т.е. за счет переходов системы из одних состояний в другие. Выполнение термодинамической работы связано только со смещением (или деформацией) уровней энергии системы без изменения распределения ее по состояниям, т.е. без изменения вероятностей Так, в случае системы, состоящей из невзаимодействующих частиц (как, например, в случае идеального газа), когда можно говорить об энергиях отдельных частиц , выполнение работы связано с изменением энергии отдельных частиц ( ) при неизменном числе частиц на каждом энергетическом уровне. Схематически на примере простейшей двух уровневой системы это показано на рис. 5.2. Напри-
) при неизменном числе частиц на каждом энергетическом уровне. Схематически на примере простейшей двух уровневой системы это показано на рис. 5.2. Напри-
 Рис. 5.2 Рис. 5.2
|
мер, при сжатии газа поршнем поршень, перемещаясь, сообщает одинаковую энергию всем сталкивающимся с ним молекулам, которые передают энергию молекулам следующего слоя и т.д. В результате возрастает энергия каждой частицы на одну и ту же величину. В качестве другого простейшего примера зависимости уровней энергии системы от ее внешнего параметра можно привести выражение для энергии микрочастицы в одномерной бесконечно глубокой потенциальной яме

где m
– масса частицы, l
– размер области движения частицы, n
– целое число, исключая нуль. Внешним параметром в данном случае является ширина ямы . При изменении ширины ямы на уровни энергии смещаются на  При увеличении ширины ямы
При увеличении ширины ямы  уровни энергии сдвигаются вниз
уровни энергии сдвигаются вниз  , а при уменьшении
, а при уменьшении  – вверх
– вверх 
В отличие от механической работы, которая равна изменению кинетической энергии тела, термодинамическая работа равна изменению его внутренней энергии.
Следует отметить также, что термодинамическая работа, как и работа механическая, совершается при протекании процесса изменения состояния, поэтому она зависит от вида процесса, и функцией состояния не является.
6.3. Работа в термодинамике
Ранее, в параграфе 6.1 мы говорили о равновесных состояниях термодинамической системы; в этих состояниях параметры системы одинаковы во всём её объёме. Приступая к рассмотрению работы в термодинамических системах, следует ожидать, что её совершение связано с изменением объёма системы. И тогда возникает вопрос, о каких же процессах идёт речь, если рассмотрению подлежат равновесные состояния? Ответ состоит в следующем: если процесс идёт медленно, то значения параметров состояния во всём объёме можно считать одинаковыми. Понятие «медленно» здесь следует уточнить. Прежде всего, оно связано с понятием «время релаксации» – временем, в течение которого устанавливается равновесие в системе. Нас сейчас интересует время выравнивания давления в системе (время релаксации), когда термодинамической системой совершается работа, связанная с изменением объёма; для однородного газа это время составляет ~ 10–16с.Очевидно, время релаксации достаточно незначительно по сравнению со временем протекания процессов в реальных термодинамических системах (или по сравнению со временем измерения). Естественно, мы вправе считать, что реальный процесс есть последовательность равновесных состояний и поэтому имеем право изобразить его линией на графике V , P (рис. 6.1.). Разумеется, по осям координатной системы могут откладываться объём и температура или давление и температура. Поскольку в алгебре, и не только, при построении графиков первой координатной осью читается и записывается х , а затем – у , т. е.«х , у », есть надежда, что читатель, прочитывая «оси координатной системы V , Р », предполагает – по оси х откладывается объём V , а по оси у – давление газа Р .
Ознакомимся с видом линий, отображающих графически простейшие процессы в системе координат, по осям которой отложены параметры состояния V , P (возможны иные координатные оси). Выбор координатной системы обусловлен тем, что площадь, ограниченная кривой процесса и двумя крайними координатами для начального и конечного значений объёма, равна работе сжатия или расширения. На рис. 6.2 приведены графики изопроцессов, проведённые из одного и того же начального состояния. Кривая адиабатического процесса (адиабата) идёт круче, чем для изотермического процесса (изотерма). Это обстоятельство можно объяснить на основании уравнения Клапейрона для состояния газов:

 (2)
(2)
Выражая из уравнения состояния Р
1 и Р
2 , разность давлений при расширении газа от объёма V
1 до объёма V
2 запишется: 
 . (3)
. (3)
Здесь, как и в уравнении (2),  .
.
При адиабатическом расширении работа над внешними телами совершается только за счёт внутренней энергии газа, вследствие чего внутренняя энергия, а вместе с ней и температура газа уменьшаются; т. е. в конце адиабатического процесса расширения (рис. 6.2) Т
2 < Т
1 (найдите обоснование); при изотермическом же процессе Т
2 Т
1 . Поэтому в формуле (3) разность давлений  при адиабатическом расширении будет больше, чем при изотермическом (проверьте, проведя преобразования).
при адиабатическом расширении будет больше, чем при изотермическом (проверьте, проведя преобразования).
Осознав, что мы имеем дело с равновесными процессами и ознакомившись с их графическим отображением в системе координат (V ,P ), перейдём к поиску аналитического выражения внешней работы, совершаемой термодинамической системой.
Абота, совершаемая системой, может быть вычислена в зависимости от значения внешних сил, действующих на систему, и от величины деформации системы – изменения её формы и размеров. Если внешние силы приложены по поверхности в виде, например, внешнего давления, сжимающего систему, то расчёт внешней работы может быть произведён в зависимости от изменения объёма системы. Для иллюстрации рассмотрим процесс расширения газа, заключённого в цилиндре с поршнем (рис. 6.3). Допустим, что внешнее давление на всех участках по поверхности цилиндра одно и то же. Если при расширении системы поршень сместился на расстояниеdl
, то элементарная работа, совершённая системой, запишется:dA
F
ds
p
S
dl
p
dV
; здесьS
– площадь поршня, аS
dl
dV
– изменение объёма системы (рис. 6.3). При расширении системы внешнее давление не всегда остаётся постоянным, поэтому работа, совершаемая  системой при изменении её объёма отV
1 доV
2 , должна рассчитываться как сумма элементарных работ, т. е. путём интегрирования:
системой при изменении её объёма отV
1 доV
2 , должна рассчитываться как сумма элементарных работ, т. е. путём интегрирования: . Из уравнения работы следует, параметры начального (p
1 ,V
1) и конечного (p
2 ,V
2) состояний системы не определяют величину совершаемой внешней работы; необходимо знать ещё и функциюр
(V
), раскрывающую изменение давления в процессе перехода системы из одного состояния в другое.
. Из уравнения работы следует, параметры начального (p
1 ,V
1) и конечного (p
2 ,V
2) состояний системы не определяют величину совершаемой внешней работы; необходимо знать ещё и функциюр
(V
), раскрывающую изменение давления в процессе перехода системы из одного состояния в другое.
В заключение следует заметить, теплообмен между системой и окружающей средой зависит не только от параметров начального и конечного состояний системы, но и от той последовательности промежуточных состояний, через которые проходит система. Это следует из первого закона термодинамики:Q U 2 –U 1 A , гдеU 1 иU 2 определяются только заданием параметров начального и конечного состояний, а внешняя работаA зависит, кроме того, ещё и от самого процесса перехода. Вследствие этого теплотаQ , полученная или отданная системой при переходе из одного состояния в другое, не может быть выражена в зависимости только от температуры её начального и конечного состояний.
Завершая экскурс в раздел «Термодинамика. Первое начало термодинамики», перечислим его ключевые понятия: термодинамическая система, термодинамические параметры, равновесное состояние, равновесный процесс, обратимый процесс, внутренняя энергия системы, первое начало термодинамики, работа термодинамической системы, адиабатический процесс.
Механическая работа
Размерность Единицы измерения СИ СГС Примечания Размерность Известные учёныеМeханическая работа - это физическая величина - скалярная количественная мера действия силы (равнодействующей сил) на тело или сил на систему тел. Зависит от численной величины и направления силы (сил), и от перемещения тела (системы тел).
Используемые обозначения
Работа обычно обозначается буквой A (от нем. A rbeit - работа, труд) или буквой W (от англ. w ork - работа, труд).
Определение
Работа силы, приложенной к материальной точке
Суммарная работа по перемещению одной материальной точки, совершаемая несколькими силами, приложенными к этой точке, определяется как работа равнодействующей этих сил (их векторной суммой). Поэтому дальше будем говорить об одной силе, приложенной к материальной точке.

При прямолинейном движении материальной точки и постоянном значении приложенной к ней силы работа (этой силы) равна произведению проекции вектора силы на направление движения и длины вектора перемещения, совершённого точкой:
A = F s s = F s c o s (F , s) = F → ⋅ s → {\displaystyle A=F_{s}s=Fs\ \mathrm {cos} (F,s)={\vec {F}}\cdot {\vec {s}}}
Здесь точкой обозначено скалярное произведение, s → {\displaystyle {\vec {s}}} - вектор перемещения; подразумевается, что действующая сила F → {\displaystyle {\vec {F}}} постоянна в течение времени, за которое вычисляется работа.
В общем случае, когда сила не постоянна, а движение не прямолинейно, работа вычисляется как криволинейный интеграл второго рода по траектории точки:
A = ∫ F → ⋅ d s → . {\displaystyle A=\int {\vec {F}}\cdot {\vec {ds}}.}
(подразумевается суммирование по кривой, которая является пределом ломаной, составленной из последовательных перемещений d s → , {\displaystyle {\vec {ds}},} если вначале считать их конечными, а потом устремить длину каждого к нулю).
Если существует зависимость силы от координат, интеграл определяется следующим образом:
A = ∫ r → 0 r → 1 F → (r →) ⋅ d r → {\displaystyle A=\int \limits _{{\vec {r}}_{0}}^{{\vec {r}}_{1}}{\vec {F}}\left({\vec {r}}\right)\cdot {\vec {dr}}} ,
где r → 0 {\displaystyle {\vec {r}}_{0}} и r → 1 {\displaystyle {\vec {r}}_{1}} - радиус-векторы начального и конечного положения тела соответственно.
- Следствие. Если направление приложенной силы ортогонально перемещению тела, или перемещение равно нулю, то работа (этой силы) равна нулю.
Работа сил, приложенных к системе материальных точек
Работа сил по перемещению системы материальных точек определяется как сумма работ этих сил по перемещению каждой точки (работы, совершённые над каждой точкой системы, суммируются в работу этих сил над системой).
Даже если тело не является системой дискретных точек, его можно разбить (мысленно) на множество бесконечно малых элементов (кусочков), каждый из которых можно считать материальной точкой и вычислить работу в соответствии с определением выше. В этом случае дискретная сумма заменяется на интеграл.
- Эти определения могут быть использованы как для вычисления работы конкретной силы или класса сил, так и для вычисления полной работы, совершаемой всеми силами, действующими на систему.
Кинетическая энергия
Кинетическая энергия вводится в механике в прямой связи с понятием работы.
Схема рассуждений такова: 1) попробуем записать работу, совершаемую всеми силами, действующими на материальную точку и, пользуясь вторым законом Ньютона (позволяющим выразить силу через ускорение), попытаться выразить ответ только через кинематические величины, 2) убедившись, что это удалось, и что этот ответ зависит только от начального и конечного состояния движения, введём новую физическую величину, через которую эта работа будет просто выражаться (это и будет кинетическая энергия).
Если A t o t a l {\displaystyle A_{total}} - полная работа, совершённая над частицей, определяемая как сумма работ, совершенных приложенными к частице силами, то она выражается как:
A t o t a l = Δ (m v 2 2) = Δ E k , {\displaystyle A_{total}=\Delta \left({\frac {mv^{2}}{2}}\right)=\Delta E_{k},}
где E k {\displaystyle E_{k}} называется кинетической энергией. Для материальной точки кинетическая энергия определяется как половина произведения массы этой точки на квадрат её скорости и выражается как:
E k = 1 2 m v 2 . {\displaystyle E_{k}={\frac {1}{2}}mv^{2}.}
Для сложных объектов, состоящих из множества частиц, кинетическая энергия тела равна сумме кинетических энергий частиц.
Потенциальная энергия
Сила называется потенциальной, если существует скалярная функция координат, известная как потенциальная энергия и обозначаемая E p {\displaystyle E_{p}} , такая что
F → = − ∇ E p . {\displaystyle {\vec {F}}=-\nabla E_{p}.}
Если все силы, действующие на частицу консервативны, и E p {\displaystyle E_{p}} является полной потенциальной энергией, полученной суммированием потенциальных энергий соответствующих каждой силе, тогда:
| F → ⋅ Δ s → = − ∇ → E p ⋅ Δ s → = − Δ E p ⇒ − Δ E p = Δ E k ⇒ Δ (E k + E p) = 0 {\displaystyle {\vec {F}}\cdot \Delta {\vec {s}}=-{\vec {\nabla }}E_{p}\cdot \Delta {\vec {s}}=-\Delta E_{p}\Rightarrow -\Delta E_{p}=\Delta E_{k}\Rightarrow \Delta (E_{k}+E_{p})=0} . |
Этот результат известен как закон сохранения механической энергии и утверждает, что полная механическая энергия в замкнутой системе, в которой действуют консервативные силы,
∑ E = E k + E p {\displaystyle \sum E=E_{k}+E_{p}}
является постоянной во времени. Этот закон широко используется при решении задач классической механики.
Работа в термодинамике
Основная статья: Термодинамическая работаВ термодинамике работа, совершенная газом при расширении, рассчитывается как интеграл давления по объёму:
A 1 → 2 = ∫ V 1 V 2 P d V . {\displaystyle A_{1\rightarrow 2}=\int \limits _{V_{1}}^{V_{2}}PdV.}
Работа, совершенная над газом, совпадает с этим выражением по абсолютной величине, но противоположна по знаку.
- Естественное обобщение этой формулы применимо не только к процессам, где давление есть однозначная функция объема, но и к любому процессу (изображаемому любой кривой в плоскости PV ), в частности, к циклическим процессам.
- В принципе, формула применима не только к газу, но и к чему угодно, способному оказывать давление (надо только чтобы давление в сосуде было всюду одинаковым, что неявно подразумевается в формуле).
Эта формула прямо связана с механической работой. Действительно, попробуем написать механическую работу при расширении сосуда, учитывая, что сила давления газа будет направлена перпендикулярно каждой элементарной площадке, равна произведению давления P на площадь dS площадки, и тогда работа, совершаемая газом для смещения h одной такой элементарной площадки будет
D A = P d S h . {\displaystyle dA=PdSh.}
Видно, что это и есть произведение давления на приращение объема вблизи данной элементарной площадкой. А просуммировав по всем dS получим конечный результат, где будет уже полное приращение объема, как и в главной формуле параграфа.
Работа силы в теоретической механике
Рассмотрим несколько детальнее, чем это было сделано выше, построение определения энергии как риманова интеграла.
Пусть материальная точка M {\displaystyle M} движется по непрерывно дифференцируемой кривой G = { r = r (s) } {\displaystyle G=\{r=r(s)\}} , где s - переменная длина дуги, 0 ≤ s ≤ S {\displaystyle 0\leq s\leq S} и на неё действует сила F (s) {\displaystyle F(s)} , направленная по касательной к траектории в направлении движения (если сила не направлена по касательной, то будем понимать под F (s) {\displaystyle F(s)} проекцию силы на положительную касательную кривой, таким образом сведя и этот случай к рассматриваемому далее). Величина F (ξ i) △ s i , △ s i = s i − s i − 1 , i = 1 , 2 , . . . , i τ {\displaystyle F(\xi _{i})\triangle s_{i},\triangle s_{i}=s_{i}-s_{i-1},i=1,2,...,i_{\tau }} , называется элементарной работой силы F {\displaystyle F} на участке G i {\displaystyle G_{i}} и принимается за приближенное значение работы, которую производит сила F {\displaystyle F} , воздействующая на материальную точку, когда последняя проходит кривую G i {\displaystyle G_{i}} . Сумма всех элементарных работ ∑ i = 1 i τ F (ξ i) △ s i {\displaystyle \sum _{i=1}^{i_{\tau }}F(\xi _{i})\triangle s_{i}} является интегральной суммой Римана функции F (s) {\displaystyle F(s)} .
В соответствии с определением интеграла Римана, можем дать определение работе:
Предел, к которому стремится сумма ∑ i = 1 i τ F (ξ i) △ s i {\displaystyle \sum _{i=1}^{i_{\tau }}F(\xi _{i})\triangle s_{i}} всех элементарных работ, когда мелкость | τ | \tau разбиения τ {\displaystyle \tau } стремится к нулю, называется работой силы F {\displaystyle F} вдоль кривой G {\displaystyle G} .
Таким образом, если обозначить эту работу буквой W {\displaystyle W} , то, в силу данного определения,
W = lim | τ | → 0 ∑ i = 1 i τ F (ξ i) △ s i {\displaystyle W=\lim _\sum _{i=1}^{i_{\tau }}F(\xi _{i})\triangle s_{i}} ,
следовательно,
W = ∫ 0 s F (s) d s {\displaystyle W=\int \limits _{0}^{s}F(s)ds} (1).
Если положение точки на траектории её движения описывается с помощью какого-либо другого параметра t {\displaystyle t} (например, времени) и если величина пройденного пути s = s (t) {\displaystyle s=s(t)} , a ≤ t ≤ b {\displaystyle a\leq t\leq b} является непрерывно дифференцируемой функцией, то из формулы (1) получим
W = ∫ a b F [ s (t) ] s ′ (t) d t . {\displaystyle W=\int \limits _{a}^{b}Fs"(t)dt.}
Размерность и единицы
Единицей измерения работы в Международной системе единиц (СИ) является джоуль, в СГС - эрг
1 Дж = 1 кг·м²/с² = 1 Н·м 1 эрг = 1 г·см²/с² = 1 дин·см 1 эрг = 10−7 Дж
Дайте пож. определение-Работа в термодинамике и Адиабатический процесс.
Cветлана
В термодинамике движение тела как целого не рассматривается и речь идет о перемещении частей макроскопического тела относительно друг друга. При совершении работы меняется объем тела, а его скорость остается раной нулю. Но скорости молекул тела меняются! Поэтому меняется температура тела. Причина в том, что при столкновении с движущимся поршнем (сжатие газа) кинетическая энергия молекул изменяется - поршень отдает часть своей механической энергии. При столкновении с удаляющимся поршнем (расширение) скорости молекул уменьшаются, газ охлаждается. При совершении работы в термодинамике меняется состояние макроскопических тел: их объем и температура.
Адиабатический процесс - термодинамический процесс в макроскопической системе, при котором система не получает и не отдаёт тепловой энергии. Линия, изображающая адиабатный процесс на какой-либо термодинамической диаграмме, называется адиабатой.
Олег гольцов
работа А=p(v1-v2)
где
p - давление создаваемое поршнем= f/s
где f-сила действующая на поршень
s - площадь поршня
примечание p=const
v1 и v2 - начальные и конечные обьемы.
Тепловые явления можно описывать с помощью величин (макроскопических параметров), регистрируемых такими приборами, как манометр и термометр. Эти приборы не реагируют на воздействие отдельных молекул. Теория тепловых процессов, в которой не учитывается молекулярное строение тел, называется термодинамикой. Об этом уже упоминалось в главе 1. В этой главе термодинамику мы будем изучать.
§ 5.1. Работа в термодинамике
В главе 3 мы познакомились с различными процессами, при которых меняется состояние термодинамической системы. У нас речь шла преимущественно об изменении состояния идеального газа при изотермическом, изобарном и изохорном процессах.
Для дальнейшего рассмотрения термодинамических процессов нужно детально исследовать, в результате каких внешних воздействий может меняться состояние любой термодинамической системы. Имеется два существенно различных вида воздействий, которые приводят к изменению состояния системы, т. е. к изменению термодинамических параметров - давления р, объема V , температуры Т, характеризующих состояние. Первый из них - это совершение работы.
Работа в механике и термодинамике
В механике рассматривается движение макроскопических тел. Работа определяется как произведение модулей силы и перемещения и косинуса угла между направлениями силы и перемещения. Работа совершается при действии силы или нескольких сил на движущееся макроскопическое тело и равна изменению его кинетической энергии.
В термодинамике движение тела как целого не рассматривается и речь идет о перемещении частей макроскопического тела друг относительно друга. При совершении работы меняется объем тела, а его скорость остается равной нулю. Но скорости молекул тела, например газа, меняются. Поэтому меняется и температура тела.
Причина состоит в следующем: при упругих соударениях молекул с движущимся поршнем (для случая сжатия газа) их кинетическая энергия изменяется. Так, при движении навстречу молекулам поршень во время столкновений передает им часть своей механической энергии, в результате чего газ нагревается. Поршень действует подобно футболисту, встречающему летящий мяч ударом ноги и сообщающему мячу скорость, значительно большую той, которой он обладал до удара*.
* Задача об изменении скорости шарика при упругом соударении его с движущейся стенкой подробно рассмотрена в § 6.12 «Механики» (задача 5).
И наоборот, если газ расширяется, то после столкновения с удаляющимся поршнем скорости молекул уменьшаются, в результате чего газ охлаждается. Так же действует футболист: чтобы уменьшить скорость летящего мяча или остановить его, нога футболиста движется от мяча, как бы уступая ему дорогу.
Итак, при совершении работы в термодинамике меняется состояние макроскопических тел: меняется их объем и температура.
Вычисление работы
Вычислим
работу в зависимости от изменения объема
на примере газа в цилиндре под поршнем
(рис. 5.1). Проще всего вначале вычислить
не работу силы
,
действующей
на газ со стороны внешнего тела (поршня),
а работу, которую совершает сам газ,
действуя на поршень с силой
 .
Согласно
третьему закону Ньютона
.
Согласно
третьему закону Ньютона

 .
.

Модуль силы, действующей со стороны газа на поршень, равен F " = pS , где р - давление газа, a S - площадь поверхности поршня. Пусть газ расширяется и поршень смещается в направлении силы на малое расстояние Δ h = h 2 – h 1 Если перемещение мало, то давление газа можно считать постоянным.
Работа газа равна:
Эту работу можно выразить через изменение объема газа. Начальный объем V 1 = Sh 1 , а конечный V 2 = Sh 2 . Поэтому

где ΔV = V 2 - V 1 - изменение объема газа.
При расширении газ совершает положительную работу, так как направления силы и перемещения поршня совпадают.
Если газ сжимается, то формула (5.1.2) для работы газа остается справедливой. Но теперь V 2 < V 1 и поэтому А" < 0 (рис. 5.2).

Работа
А, совершаемая внешними телами над
газом, отличается от работы газа А"
только знаком: А
=
-А",
так
как сила
 ,
действующая на газ, направлена против
силы
,
действующая на газ, направлена против
силы ,
а
перемещение остается тем же самым.
Поэтому работа внешних сил, действующих
на газ, равна:
,
а
перемещение остается тем же самым.
Поэтому работа внешних сил, действующих
на газ, равна:
![]() (5.1.3)
(5.1.3)
Знак минус указывает, что при сжатии газа, когда ΔV = V 2 - V 1 < 0, работа внешней силы положительна. Понятно, почему в этом случае А > 0: при сжатии газа направления силы и перемещения совпадают. При расширении газа, наоборот, работа внешних тел отрицательна (А < 0), так как ΔV = V 2 – V 1 > 0. Теперь направления силы и перемещения противоположны.
Выражения (5.1.2) и (5.1.3) справедливы не только при сжатии или расширении газа в цилиндре, но и при малом изменении объема любой системы. Если процесс изобарный (р = const), то эти формулы можно применять и для больших изменений объема.
При рассмотрении термодинамических процессов механическое перемещение макротел в целом не рассматривается. Понятие работы здесь связывается с изменением объема тела, т.е. перемещением частей макротела друг относительно друга. Процесс этот приводит к изменению расстояния между частицами, а также часто к изменению скоростей их движения, следовательно, к изменению внутренней энергии тела.
Пусть в цилиндре с подвижным поршнем находится газ при температуре T 1 (рис. 1). Будем медленно нагревать газ до температуры T 2 . Газ будет изобарически расширяться, и поршень переместится из положения 1 в положение 2 на расстояние Δl . Сила давления газа при этом совершит работу над внешними телами. Так как p = const, то и сила давления F = pS тоже постоянная. Поэтому работу этой силы можно рассчитать по формуле
\(~A = F \Delta l = pS \Delta l = p \Delta V, \qquad (1)\)
где ΔV - изменение объема газа. Если объем газа не изменяется (изохорный процесс), то работа газа равна нулю.
Сила давления газа выполняет работу только в процессе изменения объема газа .
При расширении (ΔV > 0) газа совершается положительная работа (А > 0); при сжатии (ΔV < 0) газа совершается отрицательная работа (А < 0), положительную работу совершают внешние силы А’ = -А > 0.
Запишем уравнение Клапейрона-Менделеева для двух состояний газа:
\(~pV_1 = \frac mM RT_1 ; pV_2 = \frac mM RT_2 \Rightarrow\) \(~p(V_2 - V_1) = \frac mM R(T_2 - T_1) .\)
Следовательно, при изобарном процессе
\(~A = \frac mM R \Delta T .\)
Если m = М (1 моль идеального газа), то при ΔΤ = 1 К получим R = A . Отсюда вытекает физический смысл универсальной газовой постоянной: она численно равна работе, совершаемой 1 моль идеального газа при его изобарном нагревании на 1 К.
На графике p = f (V ) при изобарном процессе работа равна площади заштрихованного на рисунке 2, а прямоугольника.
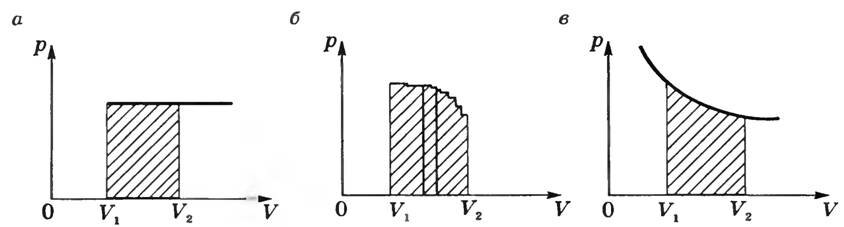
Если процесс не изобарный (рис. 2, б), то кривую p = f (V ) можно представить как ломаную, состоящую из большого количества изохор и изобар. Работа на изохорных участках равна нулю, а суммарная работа на всех изобарных участках будет
\(~A = \lim_{\Delta V \to 0} \sum^n_{i=1} p_i \Delta V_i\), или \(~A = \int p(V) dV,\)
т.е. будет равна площади заштрихованной фигуры. При изотермическом процессе (Т = const) работа равна площади заштрихованной фигуры, изображенной на рисунке 2, в.
Определить работу, используя последнюю формулу, можно только в том случае, если известно, как изменяется давление газа при изменении его объема, т.е. известен вид функции p (V ).
Таким образом, газ при расширении совершает работу. Приборы и агрегаты, действия которых основаны на свойстве газа в процессе расширения совершать работу, называются пневматическими . На этом принципе действуют пневматические молотки, механизмы для закрывания и открывания дверей на транспорте и др.
Литература
Аксенович Л. А. Физика в средней школе: Теория. Задания. Тесты: Учеб. пособие для учреждений, обеспечивающих получение общ. сред, образования / Л. А. Аксенович, Н.Н.Ракина, К. С. Фарино; Под ред. К. С. Фарино. - Мн.: Адукацыя i выхаванне, 2004. - C. 155-156.
>>Физика: Работа в термодинамике
В результате каких процессов может меняться внутренняя энергия? Вы уже знаете, что есть два вида таких процессов: совершение работы и теплопередача. Начнем с работы. Чему она равна при сжатии и расширении газа и других тел?
Работа в механике и термодинамике.
В механике
работа определяется как произведение модуля силы, модуля перемещения точки ее приложения и косинуса угла между ними. При действии силы на движущееся тело работа равна изменению его кинетической энергии.
В движение тела как целого не рассматривается, речь идет о перемещении частей макроскопического тела друг относительно друга. В результате может меняться объем тела, а его скорость остается равной нулю. Работа в термодинамике определяется так же, как и в механике, но она равна не изменению кинетической энергии тела, а изменению его внутренней энергии.
Изменение внутренней энергии при совершении работы.
Почему при сжатии или расширении тела меняется его внутренняя энергия тела? Почему, в частности, нагревается воздух при накачивании велосипедной шины?
Причина изменения температуры газа в процессе его сжатия состоит в следующем: при упругих соударениях молекул газа с движущимся поршнем изменяется их кинетическая энергия
. Так, при движении навстречу молекулам газа поршень во время столкновений передает им часть своей механической энергии, в результате чего газ нагревается. Поршень действует подобно футболисту, встречающему летящий мяч ударом ноги. Нога сообщает мячу скорость, значительно большую той, которой он обладал до удара.
И наоборот, если газ расширяется, то после столкновения с удаляющимся поршнем скорости молекул уменьшаются, в результате чего газ охлаждается. Так же действует и футболист, для того чтобы уменьшить скорость летящего мяча или остановить его, - нога футболиста движется от мяча, как бы уступая ему дорогу.
При сжатии или расширении меняется и средняя потенциальная энергия взаимодействия молекул, так как при этом меняется среднее расстояние между молекулами.
Вычисление работы.
Вычислим работу в зависимости от изменения объема на примере газа в цилиндре под поршнем (рис.13.1
).
Проще всего вначале вычислить не работу силы , действующей на газ со стороны внешнего тела (поршня), а работу, которую совершает сила давления газа, действуя на поршень с силой . Согласно третьему закону Ньютона  . Модуль силы, действующей со стороны газа на поршень, равен
. Модуль силы, действующей со стороны газа на поршень, равен ![]() , где p
- давление газа, а S
- площадь поверхности поршня. Пусть газ расширяется изобарно и поршень смещается в направлении силы на малое расстояние
, где p
- давление газа, а S
- площадь поверхности поршня. Пусть газ расширяется изобарно и поршень смещается в направлении силы на малое расстояние ![]() . Так как давление газа постоянно, то работа газа равна:
. Так как давление газа постоянно, то работа газа равна:
Эту работу можно выразить через изменение объема газа. Начальный его объем V 1 =Sh 1
, а конечный V 2 =Sh 2
. Поэтому
где - изменение объема газа.
При расширении газ совершает положительную работу, так как направление силы и направление перемещения поршня совпадают.
Если газ сжимается, то формула (13.3) для работы газа остается справедливой. Но теперь ![]() , и поэтому
, и поэтому ![]() (рис.13.2
).
(рис.13.2
).

Работа A
, совершаемая внешними телами над газом, отличается от работы самого газа A
´ только знаком: ![]() , так как сила , действующая на газ, направлена против силы а перемещение поршня остается тем же самым. Поэтому работа внешних сил, действующих на газ, равна:
, так как сила , действующая на газ, направлена против силы а перемещение поршня остается тем же самым. Поэтому работа внешних сил, действующих на газ, равна:
При сжатии газа, когда , работа внешней силы оказывается положительной. Так и должно быть: при сжатии газа направления силы и перемещения точки ее приложения совпадают.
Если давление не поддерживать постоянным, то при расширении газ теряет энергию и передает ее окружающим телам: поднимающемуся поршню, воздуху и т. д. Газ при этом охлаждается. При сжатии газа, наоборот, внешние тела передают ему энергию и газ нагревается.
Геометрическое истолкование работы.
Работе A´
газа для случая постоянного давления можно дать простое геометрическое истолкование.
Построим график зависимости давления газа от занимаемого им объема (рис.13.3
). Здесь площадь прямоугольника abdc
, ограниченная графиком p 1
=const, осью V
и отрезками ab
и cd
, равными давлению газа, численно равна работе (13.3):

В общем случае давление газа не остается неизменным. Например, при изотермическом процессе оно убывает обратно пропорционально объему (рис.13.4
). В этом случае для вычисления работы нужно разделить общее изменение объема на малые части и вычислить элементарные (малые) работы, а потом все их сложить. Работа газа по-прежнему численно равна площади фигуры, ограниченной графиком зависимости p
от V
, осью V
и отрезками ab
и cd
, равными давлениям p 1
, p 2
в начальном и конечном состояниях газа.

???
1. Почему газы при сжатии нагреваются?
2. Положительную или отрицательную работу совершают внешние силы при изотермическом процессе, изображенном на рисунке 13.2?
Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс
Содержание урока конспект урока опорный каркас презентация урока акселеративные методы интерактивные технологии Практика задачи и упражнения самопроверка практикумы, тренинги, кейсы, квесты домашние задания дискуссионные вопросы риторические вопросы от учеников Иллюстрации аудио-, видеоклипы и мультимедиа фотографии, картинки графики, таблицы, схемы юмор, анекдоты, приколы, комиксы притчи, поговорки, кроссворды, цитаты Дополнения рефераты статьи фишки для любознательных шпаргалки учебники основные и дополнительные словарь терминов прочие Совершенствование учебников и уроков исправление ошибок в учебнике обновление фрагмента в учебнике элементы новаторства на уроке замена устаревших знаний новыми Только для учителей идеальные уроки календарный план на год методические рекомендации программы обсуждения Интегрированные урокиЕсли у вас есть исправления или предложения к данному уроку,
Внутренняя энергия газа при переходе его из одного состояния в другое изменяется. Рассмотрим, как это изменение связано с работой внешних сил над газом или газа против внешних сил. Для этого рассмотрим цилиндр с подвижным поршнем. На произвольном малом участке при движении поршня изменяется объем газа и совершается работа, равная произведению силы, действующей на поршень со стороны газа, находящегося внутри цилиндра, на перемещение поршня под действием этой силы: ΔА i = F i Δx .Работа положительна, если направление силы и перемещения совпадают и отрицательна, если они противоположны. Из этого следует, что при сжатии газа положительна работа внешних сил, а при расширении положительную работу совершает газ.Для вычисления работы, совершаемой газом при изменении его объема, в определяющем уравнении работы можно заменить силу, действующую на поршень в цилиндре, через произведение давления газа на площадь поршня. Получаем, что работа в термодинамике определяется произведением давления газа на изменение его объема:
ΔA i = p i S Δx = p i ΔV .
Термодинамическая работа - способ передачи энергии, связанный с изменением внешних параметров системы.
Механическая работа определяется как:
δA =(F →dr −→), где F → - сила, а dr −→ - элементарное (бесконечно малое) перемещение.Элементарная работа термодинамической системы над внешней средой может быть вычислена так:
δA =(F →dr −→)=P (ds −→dr −→)=PdV , где ds −→ - нормаль элементарной (бесконечно малой) площадки, P - давление и dV - бесконечно малое приращение объёма. Работа в термодинамическом процессе 1→2, таким образом, выражается так: A =∫12PdV .
Величина работы зависит от пути, по которому термодинамическая система переходит из состояния 1 в состояние 2, и не является функцией состояния системы. Это легко доказать, если учесть, что геометрический смысл определённого интеграла - площадь под графиком кривой. Так как работа определяется через интеграл, то в зависимости от пути процесса площадь под кривой, а значит, и работа, будет различна. Такие величины называют функциями процесса.Несмотря на то, что до сих пор и в физической химии используется обозначение работы A , в соответствии с рекомендациями ИЮПАК работу в химической термодинамике следует обозначать как W . Впрочем, авторы могут использовать какие угодно обозначения, если только дадут им расшифровку.
Внутренняя энергия термодинамической системы может изменяться двумя способами: посредством совершения работы над системой и посредством теплообмена с окружающей средой. Энергия, которую получает или теряет тело в процессе теплообмена с окружающей средой, называется коли́чеством теплоты́ или просто теплотой . Теплота - это одна из основных термодинамических величин в классической феноменологическойтермодинамике. Количество теплоты входит в стандартные математические формулировки первого и второго начал термодинамики.Для изменения внутренней энергии системы посредством теплообмена также необходимо совершить работу. Однако это не макроскопическая работа, которая связана с перемещением границы системы. На микроскопическом уровне эта работа складывается из работ сил, действующих на молекулы системы на границе контакта более нагретого тела с менее нагретым, то есть энергия передаётся посредством столкновений молекул. Поэтому с точки зрения молекулярно-кинетической теории различие между работой и теплотой проявляется только в том, что совершение механической работы требует упорядоченного движения молекул на макроскопических масштабах, а передача энергии от более нагретого тела менее нагретому этого не требует.Энергия может также передаваться излучением от одного тела к другому и без их непосредственного контакта.Количество теплоты не является функцией состояния, и количество теплоты, полученное системой в каком-либо процессе, зависит от способа, которым она была переведена из начального состояния в конечное.Единица измерения в Международной системе единиц (СИ) - джоуль. Как единица измерения теплоты используется также калория. В Российской Федерации калория допущена к использованию в качестве внесистемной единицы без ограничения срока с областью применения «промышленность» .
Определение
Количество теплоты входит в математическую формулировку первого начала термодинамики, которую можно записать как ΔQ = A + ΔU . Здесь ΔU - изменение внутренней энергии системы, ΔQ - количество теплоты, переданное системе, а A - работа, совершённая системой. Однако определение теплоты должно указывать способ её измерения безотносительно к первому началу. Так как теплота - это энергия переданная в ходе теплообмена, для измерения количества теплоты необходимо пробное калориметрическое тело. По изменению внутренней энергии пробного тела можно будет судить о количестве теплоты, переданном от системы пробному телу. Без использования пробного тела первое начало теряет смысл содержательного закона и превращается в бесполезное для расчётов определение количества теплоты.Пусть в системе, состоящей из двух тел X и Y , тело Y (пробное) заключено в жёсткую адиабатическую оболочку. Тогда оно не способно совершать макроскопическую работу, но может обмениваться энергией (то есть теплотой) с телом X . Предположим, что тело X также почти полностью заключено в адиабатическую, но не жёсткую оболочку, так что оно может совершать механическую работу, но обмениваться теплотой может лишь сY . Количеством теплоты , переданным телу X в некотором процессе, называется величина Q X = −ΔU Y , где ΔU Y - изменение внутренней энергии тела Y . Согласно закону сохранения энергии, полная работа, выполненная системой, равна убыли полной внутренней энергии системы двух тел: A = −ΔU x − ΔU y , где A - макроскопическая работа, совершенная телом X , что позволяет записать это соотношение в форме первого начала термодинамики: ΔQ = A +ΔU x .Таким образом, вводимое в феноменологической термодинамике количество теплоты может быть измерено посредством калориметрического тела (об изменении внутренней энергии которого можно судить по показанию соответствующего макроскопического прибора). Из первого начала термодинамики следует корректность введённого определения количества теплоты, то есть независимость соответствующей величины от выбора пробного тела Y и способа теплообмена между телами. При таком определении количества теплоты первое начало становится содержательным законом, допускающим экспериментальную проверку, так как все три величины, входящие в выражение для первого начала, могут быть измерены независимо.
Первое начало термодинамики - один из трёх основных законов термодинамики, представляет собой закон сохранения энергии для термодинамических систем.Первое начало термодинамики было сформулировано в середине XIX века в результате работ немецкого учёного Ю. Р. Майера, английского физика Дж. П. Джоуля и немецкого физика Г. Гельмгольца . Согласно первому началу термодинамики, термодинамическая система может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источников энергии. Первое начало термодинамики часто формулируют как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника.
